Fique por dentro de tudo!
Participe do nosso canal direto no WhatsApp para receber em primeira mão as novidades, lançamentos e oportunidades exclusivas da Kasvi.
6 min de leitura
O Southern Blotting ou Blot, foi batizado com o nome de seu inventor, Edward M. Southern que o desenvolveu para identificar sequências específicas de DNA. Pode ser usado para detectar a identidade, o tamanho e a abundância do DNA em uma mostra. Se um cientista quer saber se um organismo tem uma mutação genética particular, o Southern Blotting pode ser usado para identificar a presença desse gene mutante. A metodologia consiste na fragmentação do DNA em pedaços menores, através de uma eletroforese, seguindo-se a transferência para uma membrana e a detecção do fragmento de DNA de interesse por hibridação com uma sonda específica.
 |
As outras técnicas de transferência emergiram deste método e foram denominadas Northern Blotting (para RNA) e Western Blotting (para proteínas). |
A primeira etapa é a fragmentação ou digestão do DNA, onde as longas sequências de nucleotídeos devem ser divididas em fragmentos menores com a ajudas das endonucleases ou enzimas de restrição. Cada enzima reconhece uma ou mais sequências alvo e corta o DNA nestas sequências ou perto delas. O corte é escalonado, produzindo terminações com DNA fita simples.
 |
Uma das primeiras enzimas de restrição a ser isolada foi a EcoRI, foi produzida pela bactéria Escherichia coli. Essa enzima reconhece apenas a sequência GAATTC |
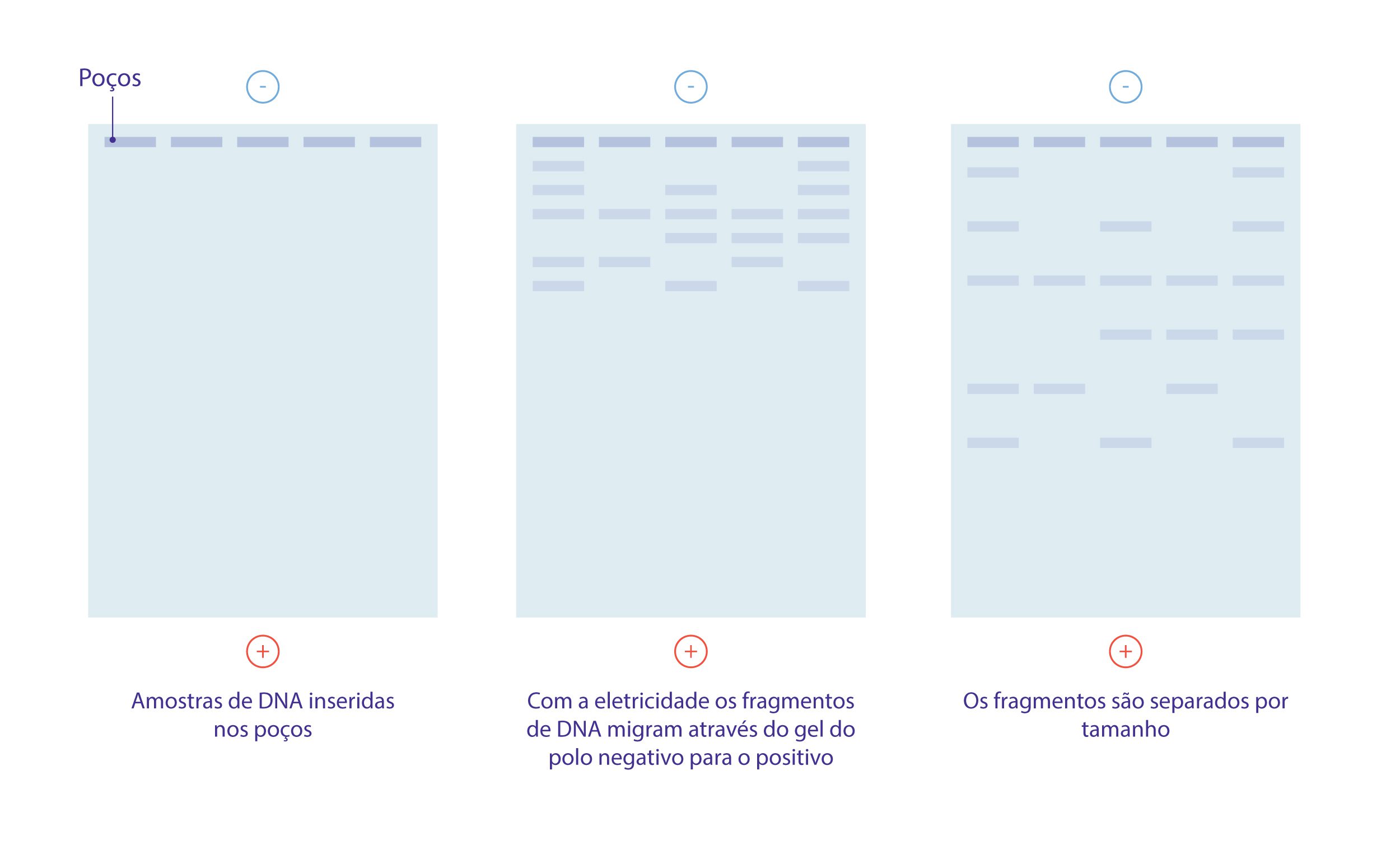
O DNA fragmentado é submetido a eletroforese em gel de agarose para separar os fragmentos de acordo com peso molecular à medida que passam por uma corrente elétrica.
Todas as moléculas de DNA têm a mesma quantidade de carga por massa. Por essa razão, a eletroforese em gel de fragmentos de DNA faz a separação baseada apenas no tamanho. Através do uso da eletroforese, podemos ver quantos diferentes fragmentos de DNA estão presentes em uma amostra, e o quão grande eles são em relação aos outros. Podemos também determinar o tamanho absoluto de um pedaço de DNA examinando-o ao lado de um DNA “padrão”, composto de fragmentos de DNA de tamanhos conhecidos.
Para transferência do DNA separado no gel para uma membrana de nitrocelulose ou de nylon, é necessário colocar a membrana sobre o gel e aplicar pressão uniformemente distribuída sobre o gel, levando à ligação do DNA à membrana. Seguidamente, a membrana é aquecida (no caso da utilização de uma membrana de nitrocelulose) ou exposta a radiação UV (no caso da utilização de uma membrana de nylon) para fixar permanentemente o DNA à membrana.
Recomenda-se a utilização de membranas de nylon devido à sua capacidade de se ligar mais eficientemente ao DNA.
A sonda é um pequeno pedaço de DNA que é projetada para ter uma sequência complementar a sequência particular do DNA na amostra. Isto permite que a sonda hibride ou se ligue a um fragmento de DNA específico na membrana. Além disso, a sonda possui um marcador, que normalmente é um átomo radioativo ou um corante fluorescente.
A técnica de hibridação é importante para analisar genes expressos assim como genes não expressos na amostra. A visualização destes genes de interesse dá-se pelo emparelhamento das sondas que se encontram marcadas.
Assim, após a hibridação, a sonda permite que o fragmento de DNA de interesse seja detectado entre os muitos fragmentos de DNA diferentes na membrana. Essa sonda irá parear com qualquer sequência de DNA complementar a ela. Portanto se a sequência procurada não estiver presente na amostra não houve o pareamento.
O excesso de sonda é lavado da membrana, e toda a sonda não hibridizada será removida. Depois disso, a presença ou não da sonda na membrana (e as posições onde ela está presente) é revelada por uma autorradiografia em um filme de raio-X, ou pelo aparecimento de uma cor caso um marcador cromogênico tenha sido usado.
Assim como computadores, telefones celulares e carros se tornam tecnologicamente mais avançados, deixando as versões anteriores obsoletas, algumas técnicas laboratoriais são substituídas por versões aprimoradas que economizam tempo e dinheiro. No entanto, as técnicas tradicionais e até mesmo históricas, não deixam de perder sua importância no campo científico.
Hoje, o Southern blotting pode ser substituído pelo PCR em tempo real para responder às mesmas questões experimentais. O PCR em tempo real detecta e quantifica um gene ou sequência de DNA de interesse registrando a abundância de DNA ao longo do processo de amplificação. Isso permite ao pesquisador comparar diferentes sequências de DNA para ver qual é mais abundante em uma amostra.
O Southern blotting é intensivo em mão-de-obra e requer uma grande quantidade de DNA de alta qualidade, enquanto que no PCR em tempo real a automação é mais fácil, a quantidade de DNA necessário é bem menor, além da economia do tempo e recursos. Porém, e metodologia Southern blotting a taxa de falsos positivos é mais baixa do que o PCR em tempo real.
